Menyediakan produk berkualitas tinggi berarti memproduksi setiap unit agar aman, efektif, dan bebas dari kontaminasi atau cacat.
Di sinilah Sistem Manajemen Mutu (SMM) yang tepat berperan. SMM yang menggabungkan GxP dan Manajemen Risiko Mutu dapat memantau efektivitas proses produksi. Sistem mutu efektif ketika produsen mengidentifikasi masalah dengan cepat dan menerapkan tindakan korektif dan pencegahan. Oleh karena itu, komponen utama dari setiap sistem mutu adalah bagaimana Anda menangani penyimpangan .
Hari ini, kita akan membahas cara menangani penyimpangan dalam farmasi dan cara melakukan analisis akar penyebab , investigasi, kesimpulan, dan tindak lanjut yang sesuai.
Apa itu penyimpangan?
Penyimpangan didefinisikan sebagai setiap perbedaan terukur antara nilai yang diamati dan nilai yang diharapkan atau 'normal' untuk suatu proses atau kondisi produk, atau penyimpangan dari standar, instruksi, prosedur, atau spesifikasi yang disetujui. Titik di mana penyimpangan dari norma tersebut menjadi penyimpangan yang sebenarnya harus didefinisikan.
Penyimpangan vs Ketidaksesuaian
Ketidaksesuaian
Ketidaksesuaian adalah ketidakpatuhan terhadap persyaratan tertentu. Perlu diingat bahwa pedoman ISO telah menghapus kata "ketidaksesuaian", oleh karena itu istilah yang paling tepat adalah "ketidaksesuaian" .
Ketidaksesuaian dapat terjadi pada produk dan proses. Dengan demikian, proses yang tidak sesuai dapat menyebabkan produk yang tidak sesuai. Dengan demikian, kejadian ini harus diselidiki dan diselesaikan secara menyeluruh untuk mencegah terulangnya kembali.
Sebagai contoh ketidaksesuaian:
Bila analisis kendali mutu menentukan bahwa kemurnian suatu produk obat tidak memenuhi spesifikasi, maka hasil ketidaksesuaian tersebut dikategorikan sebagai ketidaksesuaian. Produk tersebut tidak akan disetujui dalam kasus ini. Sebaliknya, produk tersebut akan dimusnahkan, karena tidak ada cara untuk memprosesnya kembali.
Deviasi
Ada dua jenis penyimpangan: terencana dan tidak terencana.
- Penyimpangan terencana adalah penyimpangan atau perubahan jangka pendek dari proses atau prosedur yang ada yang dimaksudkan untuk dijalankan secara terkendali, sebagai bagian dari validasi proses baru. Penyimpangan ini disengaja dan telah disetujui sebelumnya oleh Jaminan Mutu sebelum pelaksanaan. Penting untuk digarisbawahi bahwa penyimpangan terencana bukanlah pengganti Manajemen Perubahan. Pedoman saat ini menyatakan bahwa setiap penyimpangan dari instruksi atau prosedur harus dihindari sebisa mungkin. Namun, beberapa penyimpangan terencana terjadi dan diperbolehkan dengan alasan yang jelas.
- Penyimpangan yang tidak direncanakan sesuai dengan setiap penyimpangan dari instruksi atau standar yang disetujui yang muncul secara tidak terduga, karena kesalahan manusia, kegagalan peralatan, atau kegagalan fungsi.
Cara menangani penyimpangan dalam farmasi
Alur kerja proses manajemen penyimpangan dapat berbeda dari satu organisasi ke organisasi lain, tergantung pada apakah Anda menggunakan sistem manajemen mutu berbasis kertas atau elektronik . Biasanya, kami membagi proses penyimpangan menjadi enam fase:
- Tahap 1: Identifikasi dan pelaporan penyimpangan
- Tahap 2: Investigasi dan analisis akar penyebab
- Tahap 3: Penilaian risiko
- Tahap 4: Rencana Aksi (CAPA)
- Tahap 5: Pemeriksaan efektivitas CAPA
- Tahap 6: Tinjauan berkala
Identifikasi dan pelaporan penyimpangan
Pada tahap pertama, data dan bukti awal dikumpulkan. Penyimpangan didokumentasikan berdasarkan prosedur internal. Paling tidak, hal-hal berikut harus dicatat:
- Nama pengamatan
- Nama pemberi tahu ditambah tanggal dan waktu
- Nama dan ID peralatan dan produk yang terkena dampak
- Status proses pada saat peristiwa terjadi
- Deskripsi singkat tentang prosedur atau standar yang menyimpang, kemungkinan akar penyebabnya, dll.
- Jenis penyimpangan diidentifikasi: insiden, minor, major, atau kritis berdasarkan prinsip Sistem Manajemen Risiko.
- Tindakan segera telah diambil
Alternatifnya, Anda dapat mengidentifikasi penyimpangan berdasarkan pendekatan 5W1H . Daftar periksa atau templat yang telah ditetapkan sebelumnya direkomendasikan dalam fase ini.
Karyawan harus dilatih untuk memahami proses penyimpangan sehingga mereka dapat melaporkan segera setelah mereka menyimpang, melakukan kesalahan, atau menyadari sesuatu yang tidak biasa, sebaiknya pada tanggal terjadinya.
Langkah awal ini juga memainkan peran penting dalam menangani proses CAPA karena ini mencakup identifikasi masalah yang memerlukan tindakan perbaikan. Ini juga mengidentifikasi sumber yang digunakan untuk mengklasifikasikan masalah yang terjadi.
Terkadang, perbaikan segera dilakukan sebelum investigasi selesai dan akar permasalahan ditentukan. Ini karena tindakan segera dapat mengurangi risiko serius atau masalah keselamatan. Jika ada tindakan segera (perbaikan) yang dilakukan, tindakan tersebut harus didokumentasikan selama fase identifikasi.
Identifikasi dan pelaporan penyimpangan
Setiap penyimpangan yang signifikan harus dicatat dan diselidiki secara menyeluruh, untuk menentukan akar penyebabnya dan tindakan korektif dan pencegahan yang tepat (Eudralex: Bab 1.8, VII). Penyimpangan tersebut harus diidentifikasi dan dilaporkan oleh personel yang terlibat dalam proses yang relevan. Namun, hanya individu yang memenuhi syarat yang boleh diberi wewenang untuk mengeluarkan kejadian tersebut. Selain itu, laporan investigasi harus disetujui oleh orang yang kompeten, biasanya seorang manajer QA. Jika manajer QA tidak ada, seorang penanggung jawab cadangan dapat mengevaluasi laporan tersebut.
Investigasi merupakan salah satu fase terpenting (dan tersulit) dari proses ini. Biasanya, analisis akar penyebab tidak diperlukan jika kejadian tersebut dikategorikan sebagai insiden atau minor. Namun, jika kejadian tersebut mayor atau lebih tinggi, dan akar penyebabnya tidak diketahui, investigasi menyeluruh harus dilakukan menggunakan alat analisis akar penyebab.
Tujuannya adalah untuk menentukan alasan utama mengapa suatu masalah terjadi dan yang menyebabkan ketidaksesuaian atau penyimpangan yang tidak direncanakan. Pendekatan ini sering disebut analisis akar penyebab (RCA) yang merupakan proses pemecahan masalah yang sistematis.
RCA yang efektif memerlukan pemikiran kritis dan tim ahli multidisiplin untuk memeriksa setiap sudut pandang. Oleh karena itu, tim pengarah ditugaskan untuk setiap penyimpangan, dengan perwakilan dan pemilik dari semua area fungsional. Setiap anggota tim dapat menawarkan keahlian mereka untuk memandu investigasi.
Dari sana, penyimpangan dapat diselidiki secara menyeluruh dan akar penyebabnya dapat segera diperbaiki.
Prinsip RCA dan Manajemen Risiko Mutu harus diterapkan selama investigasi. Ada beberapa alat dan teknik yang dapat diandalkan untuk menganalisis akar penyebabnya, termasuk:
- FMEA (Analisis Mode dan Efek Kegagalan)
- Pemetaan Proses
- Analisis Pohon Kesalahan (FTA)
- Diagram Tulang Ikan (Penyebab dan Akibat atau Ishikawa)
- 5 Mengapa
Kadang-kadang, meskipun semua ahli subjek terlibat dan semua alat dan teknik yang tepat digunakan, akar penyebab sebenarnya dari ketidaksesuaian/penyimpangan tidak dapat ditentukan. Dalam kasus ini, pertimbangan diberikan pada akar penyebab yang paling mungkin sehingga akar penyebab tersebut dapat diatasi.
Akar penyebabnya bisa berasal dari berbagai jenis kesalahan termasuk:
- Manusia
- Bahan
- Pengukuran
- Lingkungan
- Metode
- Mesin
Penilaian risiko
Otoritas kesehatan dan panduan peraturan mendorong organisasi untuk mengklasifikasikan penyimpangan/ketidaksesuaian berdasarkan kriteria manajemen risiko mutu.
Klasifikasi berbasis risiko dari suatu kejadian menentukan tingkat kekritisannya. Klasifikasi ini juga membantu menentukan tingkat dan cakupan investigasi serta upaya yang diperlukan untuk menyelidiki suatu kejadian. Hal ini penting, karena tidak ada sumber daya yang tidak terbatas untuk menyelidiki setiap kejadian. Anda cukup berfokus pada kejadian yang paling kritis.
Setelah akar permasalahan ditentukan, fase ini memeriksa dampak akar permasalahan pada produk dalam kelompok lain yang mungkin terpengaruh oleh kejadian tersebut. Ketidaksesuaian dapat menyebabkan penyimpangan lainnya.
Misalnya, jika penyimpangan terkait dengan kerusakan instrumen selama produksi batch (misalnya, pH meter), maka semua batch yang diproduksi sejak pemeriksaan kalibrasi terakhir harus disertakan dalam investigasi.
Investigasi ini dapat dengan mudah disesuaikan jika Anda menggunakan Sistem Manajemen Mutu Elektronik, karena mengintegrasikan kejadian dengan isu lain (misalnya, kontrol perubahan, tanggal kalibrasi, investigasi lain, dll.).
Secara umum, penilaian risiko adalah alat pemeringkatan risiko, menggunakan sistem penilaian, yang membantu mengkategorikan suatu peristiwa berdasarkan kriteria yang telah ditetapkan sebelumnya.
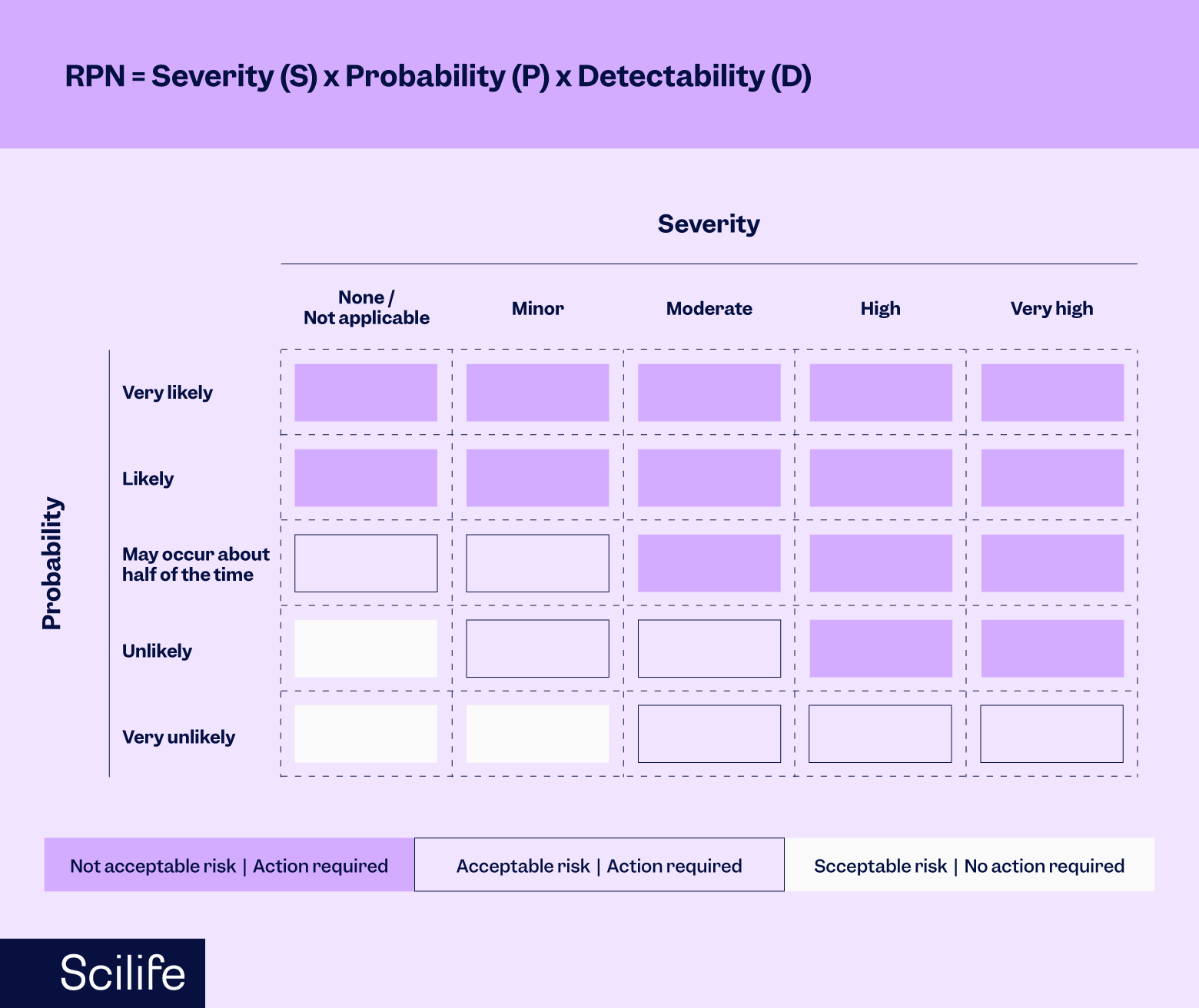
Anda dapat menggunakan alat penilaian risiko yang disebut FMEA (Failure Modes and Effects Analysis) untuk mengkategorikan penyimpangan. Model FMEA menghitung peringkat risiko menggunakan tiga faktor: Severity (S), Probability of Occurrence (P atau O), dan Detectability (D).
Misalnya,
- Probabilitas (P), atau kemungkinan, dapat dinilai sebagai berikut:

- Detectability (D), pendekatan serupa dapat digunakan.
- Tingkat keparahan dapat diterapkan untuk mengukur dampak pada atribut kualitas. Hal ini juga dapat digunakan untuk menilai potensi risiko terhadap kesehatan manusia, serta risiko kehilangan pelanggan. Tingkat keparahan juga dapat digunakan untuk menilai risiko lingkungan, dll.

Penilaian risiko diperoleh dengan mengalikan Tingkat Keparahan (S), Probabilitas (P) Kejadian, dan Kemampuan Deteksi (D) untuk mengidentifikasi tingkat kekritisan. Anda harus menetapkan setidaknya 2 tingkat untuk apa yang dapat diterima dan apa yang tidak dapat diterima berdasarkan produk Anda.
Membangun rencana aksi CAPA
Setelah analisis akar penyebab selesai dan penyebab yang menyebabkan kejadian ditemukan, tindakan korektif dan preventif (CAPA) yang tepat harus diidentifikasi dan didokumentasikan dalam respons rencana tindakan terhadap investigasi. Tindakan korektif diambil untuk memperbaiki masalah, sementara tindakan preventif diambil untuk mencegah penyimpangan dan ketidaksesuaian. Bergantung pada hasil penilaian risiko, terkadang tidak diperlukan tindakan apa pun.
Tips dan Rekomendasi
Pada bagian sebelumnya, kita membahas cara menangani penyimpangan, melakukan investigasi, dan melakukan analisis akar penyebab. Setelah Anda melakukan semuanya dengan benar hingga langkah ini, saatnya untuk menjalankan tindakan yang telah Anda rencanakan. Ini seharusnya sangat mudah karena Anda telah menemukan akar penyebab dan merencanakan tindakan untuk mengatasinya.
Namun, pentingnya pemeriksaan efektivitas tindakan yang diambil sering kali diabaikan dan diremehkan.
Pemeriksaan efektivitas CAPA
Efektivitas CAPA harus dipantau dan dinilai secara berkala.
Auditor dan inspektur mengharapkan produsen untuk menunjukkan bahwa sistem mutu mereka efektif. Suatu sistem harus mampu mengidentifikasi masalah dengan cepat dan menerapkan tindakan pencegahan dan perbaikan yang efektif, tetapi pada saat yang sama juga mampu menunjukkan bahwa sistem tersebut efektif. Oleh karena itu, sistem harus memiliki sistem verifikasi efektivitas bawaan untuk memeriksa tindakan yang diambil.
Ingatlah bahwa fase ini sesuai dengan fase “C” (Check) dari Siklus Deming: PDCA (Plan, Do, Check, dan Act) . Jika proses CAPA tidak berhasil atau hanya berhasil sebagian, proses CAPA lainnya harus dimulai.
Selain itu, jika tindakan tersebut merupakan perubahan dalam proses, aktivitas validasi atau validasi ulang tambahan mungkin diperlukan. Aktivitas validasi tersebut menghasilkan data dan bukti untuk mengonfirmasi efektivitas tindakan yang diambil guna menghilangkan pengulangan penyimpangan atau ketidaksesuaian di masa mendatang.
Tinjauan berkala
Tinjauan berkala terus memantau apakah penyimpangan dan ketidaksesuaian terjadi lagi. Fase ini menentukan status validasi dan tindakan yang diperlukan untuk mempertahankan status sistem atau peralatan yang tervalidasi. Hal ini dimaksudkan untuk menunjukkan bahwa semuanya terkendali. Data yang dipantau memastikan proses tetap sesuai untuk tujuan penggunaannya.
Tinjauan berkala digunakan untuk memeriksa semua kejadian penting, investigasi terkait, dan efektivitas tindakan perbaikan dan pencegahan yang diambil. Tinjauan dapat dilakukan berdasarkan jenis produk atau proses, peralatan, departemen, dll.
Misalnya, departemen tempat kejadian bermula harus mengumpulkan data selama periode tertentu terkait efektivitas tindakan yang diterapkan. Jaminan Mutu juga dapat dilibatkan dalam peninjauan untuk memeriksa efektivitas tindakan yang diambil dan untuk memastikan tidak ada masalah tambahan yang muncul akibat perubahan tersebut.
Kesimpulan
Kesimpulannya, melakukan analisis akar penyebab secara menyeluruh dan menangani penyimpangan secara efektif merupakan elemen penting dalam menjaga integritas sistem manajemen mutu. Tulisan blog ini telah membahas langkah-langkah penting yang terlibat—mulai dari mengidentifikasi dan melaporkan penyimpangan hingga menyelidikinya dan menerapkan tindakan korektif dan pencegahan (CAPA). Setiap fase sangat penting dalam memastikan bahwa mutu, keamanan, dan kemanjuran produk tidak terganggu.
Penting untuk diingat bahwa sistem penanganan penyimpangan yang dikelola dengan baik tidak boleh dilihat sebagai biaya, tetapi sebagai investasi dalam jaminan kualitas, manajemen risiko, dan keselamatan pasien. Dengan menggunakan prinsip-prinsip yang diuraikan dalam artikel ini, produsen dapat memastikan bahwa produk mereka secara konsisten memenuhi standar kualitas tinggi yang diperlukan untuk penggunaan medis dengan mematuhi kondisi kontrol yang tidak hanya memenuhi tetapi juga melampaui standar regulasi.





Tidak ada komentar:
Posting Komentar